
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Ostatnio zmodyfikowany 2025-01-22 17:07.
Dlaczego jest Układ okresowy pierwiastków uporządkowany według liczby atomowej i nie masa atomowa ? Liczba atomowa jest numer protonów w jądrze każdego atomy pierwiastka . To numer jest unikalny dla każdego element . Masa atomowa jest określana przez numer protonów i neutronów łącznie.
Podobnie, czy układ okresowy jest uporządkowany według liczby atomowej?
ten układ okresowy pierwiastków pierwiastków porządkuje wszystkie znane pierwiastki chemiczne w tablicy informacyjnej. Elementy są ułożone od lewej do prawej i od góry do dołu w kolejności rosnącej Liczba atomowa . Zamówienie generalnie pokrywa się ze wzrostem masa atomowa . Wiersze nazywane są okresami.
Po drugie, dlaczego tabela jest okresowa? Nazywa się „ okresowy ponieważ pierwiastki są uszeregowane w cyklach lub okresach. Od lewej do prawej pierwiastki są uszeregowane w rzędach na podstawie ich liczby atomowej (liczby protonów w ich jądrze). Niektóre kolumny są pomijane w celu uzyskania pierwiastków o tej samej liczbie wartościowości elektrony ustawiają się na tych samych kolumnach.
Ponadto, dlaczego układ okresowy jest zorganizowany przez zwiększanie liczby atomowej, a nie przez zwiększanie masy atomowej?
Liczba atomowa jako podstawa do Okresowy Prawo Zakładając, że wystąpiły błędy w masy atomowe Mendelejew umieścił pewne elementy nie w kolejności zwiększenie masy atomowej aby pasowały do odpowiednich grup (podobne elementy mają podobne właściwości) jego układ okresowy pierwiastków.
Co to jest liczba masowa atomowa?
ten Liczba masowa (symbol A, od niemieckiego słowa Atomgewicht [ atomowy waga]), zwany także liczba masowa atomowa lub nukleon numer , to suma numer protonów i neutronów (zwanych łącznie nukleonami) w an atomowy jądro. ten Liczba masowa jest inny dla każdego izotopu pierwiastka chemicznego.
Zalecana:
Jaki jest okresowy trend wielkości atomowej od góry do dołu w grupie?

Od góry do dołu w dół grupy elektroujemność maleje. Dzieje się tak, ponieważ liczba atomowa wzrasta w dół grupy, a zatem zwiększa się odległość między elektronami walencyjnymi a jądrem lub większy promień atomowy
Czym są liczby naturalne liczby całkowite i liczby wymierne?
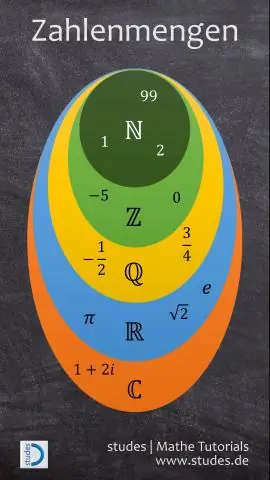
Liczby rzeczywiste dzieli się głównie na liczby wymierne i niewymierne. Liczby wymierne obejmują wszystkie liczby całkowite i ułamki. Wszystkie ujemne liczby całkowite i liczby całkowite składają się na zbiór liczb całkowitych. Liczby całkowite składają się ze wszystkich liczb naturalnych i zera
Jak zaprojektowany jest układ okresowy pierwiastków?
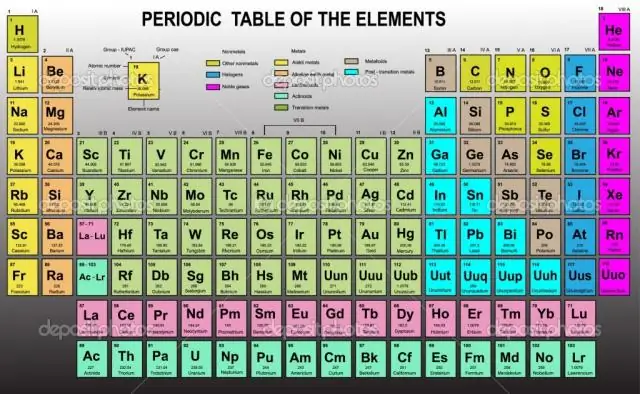
Zasługa za stworzenie układu okresowego przypada na ogół chemikowi Dmitrijowi Mendelejewowi. W 1869 r. wypisał znane pierwiastki (których było wówczas 63) na kartach i ułożył je w kolumny i rzędy według ich właściwości chemicznych i fizycznych
Jaki jest układ elektronów dla liczby atomowej potasu 19)?

Kiedy napiszemy konfigurację, umieścimy wszystkie 19 elektronów na orbitalach wokół jądra Potassumatomu. W tym filmie użyjemy wykresu konfiguracji elektronów, aby pomóc nam napisać notację dla potasu. Zauważ, że ostatni wyraz w konfiguracji elektronu potasu będzie 1s2 2s2 2p6 3s2 3p6 4s1
Dlaczego układ okresowy pierwiastków jest uporządkowany według liczby atomowej, a nie masy atomowej?

Dlaczego układ okresowy jest uporządkowany według liczby atomowej, a nie masy atomowej? Liczba atomowa to liczba protonów w jądrze atomów każdego pierwiastka. Numer ten jest unikalny dla każdego elementu. Masę atomową określa łączna liczba protonów i neutronów
