
- Autor Miles Stephen stephen@answers-science.com.
- Public 2023-12-15 23:39.
- Ostatnio zmodyfikowany 2025-01-22 17:07.
Prawo gazu doskonałego, jak to się mówi, jest tak naprawdę PV = nRT , ze wszystkimi standardowymi zmiennymi. Tutaj n=m/M, gdzie m jest masą gazu, a M masą cząsteczkową gazu. W skrócie R w PV = nRT jest pomniejszany o współczynnik M (masa cząsteczkowa), aby otrzymać R w PV = mRT.
Po prostu, co jest równe rw pV nRT?
Idealne prawo gazu to: pV = nRT , gdzie n to liczba moli, a r jest uniwersalną stałą gazową. Wartość r zależy od zaangażowanych jednostek, ale zwykle jest określane z jednostkami S. I. jako: r = 8,314 J/mol. Oznacza to, że dla powietrza możesz użyć wartości r = 287 J/kg.
Podobnie, co oznacza R w chemii pV nRT? Jednostki uniwersalnej stałej gazowej r pochodzi z równania PV=n r T. Ono stoiska dla Regnault.
W związku z tym, co oznacza N w pV nRT?
. Prawo fizyczne opisujące zależność mierzalnych właściwości gazu doskonałego, gdzie P (ciśnienie) × V (objętość) = (liczba moli) × R (stała gazowa) × T (temperatura w kelwinach). Wywodzi się z połączenia praw gazowych Boyle'a, Charlesa i Avogadro. Zwane także uniwersalnym prawem gazowym.
Czym jest M w prawie gazu doskonałego?
Oryginalny idealne prawo gazu używa wzoru PV =nRT, wersji gęstości idealne prawo gazu to PM = dRT, gdzie P to ciśnienie mierzone w atmosferach (atm), T to temperatura mierzona w kelwinach (K), R to idealne prawo gazu stała0,0821 w m (L) m ol(K) tak jak w oryginalnym wzorze, ale m jest teraz masą molową (g m stary
Zalecana:
Jaka jest różnica między dyfuzją osmozy a dyfuzją ułatwioną?

Osmoza występuje również, gdy woda przemieszcza się z jednej komórki do drugiej. Z drugiej strony dyfuzja ułatwiona ma miejsce, gdy środowisko otaczające komórkę ma większe stężenie jonów lub cząsteczek niż środowisko wewnątrz komórki. Cząsteczki przemieszczają się z otaczającego środowiska do komórki dzięki gradientowi dyfuzji
Jaka jest różnica między korelacją a kwadratem chi?
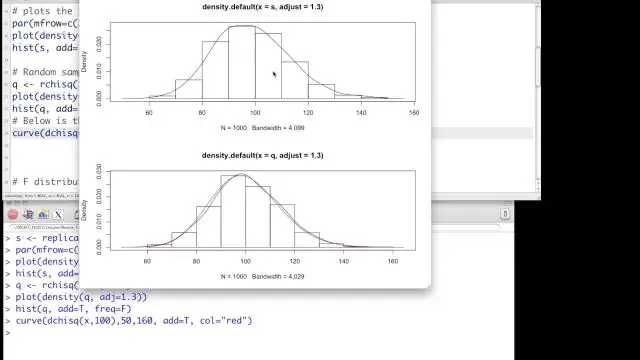
Tak więc korelacja dotyczy liniowej zależności między dwiema zmiennymi. Zwykle oba są ciągłe (lub prawie), ale istnieją odmiany w przypadku, gdy jeden jest dychotomiczny. Chi-kwadrat dotyczy zwykle niezależności dwóch zmiennych. Zwykle oba są kategoryczne
Jaka jest różnica między strefą klimatyczną a biomem?

Klimat jest klasyfikowany na podstawie temperatury atmosferycznej i opadów, podczas gdy biom jest klasyfikowany przede wszystkim na podstawie jednolitych rodzajów roślinności. Klimat może określić, jaki biom jest obecny, ale biom zazwyczaj nie kontroluje ani nie wpływa na klimat w ten sam sposób
Co to jest wzór strukturalny Jaka jest różnica między wzorem strukturalnym a modelem molekularnym?
Wzór cząsteczkowy wykorzystuje symbole chemiczne i indeksy dolne, aby wskazać dokładną liczbę różnych atomów w cząsteczce lub związku. Wzór empiryczny podaje najprostszy, całkowity stosunek atomów w związku. Wzór strukturalny wskazuje układ wiązań atomów w cząsteczce
Jaka jest różnica między prędkością chwilową a średnią, co jest najlepszym przykładem prędkości chwilowej?

Średnia prędkość to prędkość uśredniona na przestrzeni czasu. Prędkość chwilowa to prędkość w dowolnej chwili w tym przedziale czasu, mierzona za pomocą prędkościomierza w czasie rzeczywistym
